
Закон сохранения массы веществ

Определите валентность элементов
1 вариант FeF 3 , MgS , K 2 S , SO 2
2 вариант Fe 2 S 3 , H 2 S , CaO , Ag 2 S
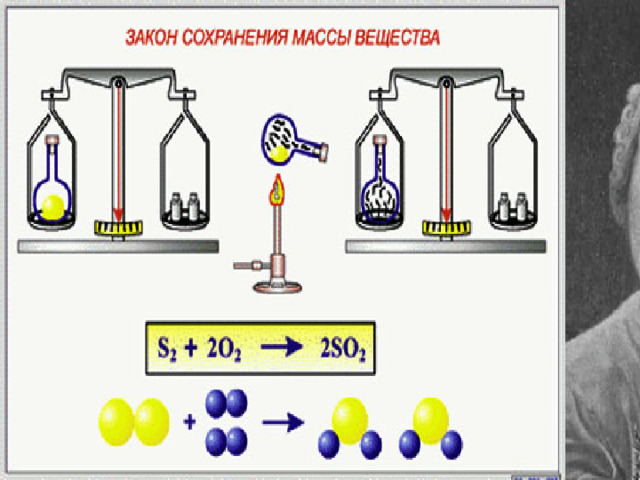

Формулировка закона
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
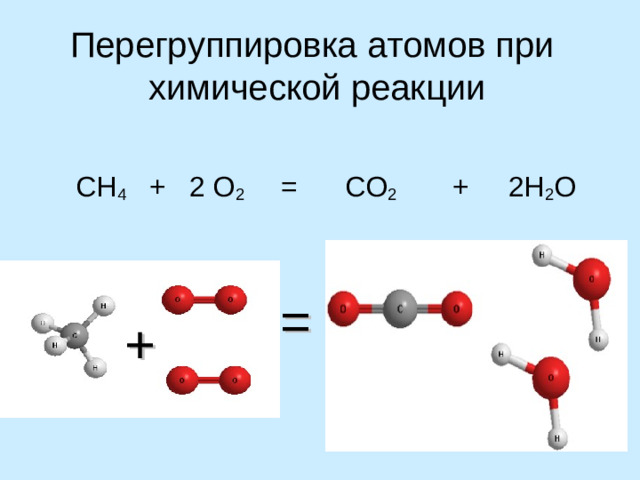
Перегруппировка атомов при химической реакции
СН 4 + 2 О 2 = СО 2 + 2Н 2 О
=
+

Алгоритм расстановки коэффициентов в уравнении химической реакции.
1. Подсчитать количество атомов каждого элемента в правой и левой части .
2. Начинать лучше с атомов О или любого другого неметалла, и начинать считать по тому, кого в левой части больше
3. Подобрать коэф-ты, чтобы атомов всех хим. элементов слева и права было одинаково
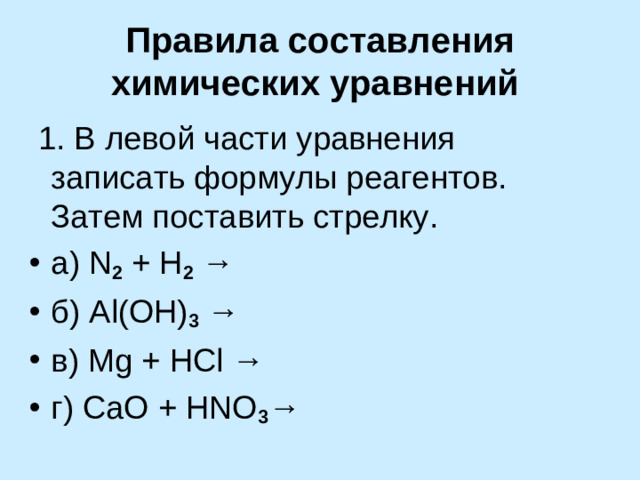
Правила составления химических уравнений
1. В левой части уравнения записать формулы реагентов. Затем поставить стрелку.
- а) N 2 + H 2 →
- б) Al ( OH ) 3 →
- в) Mg + HCl →
- г) С aO + HNO 3 →
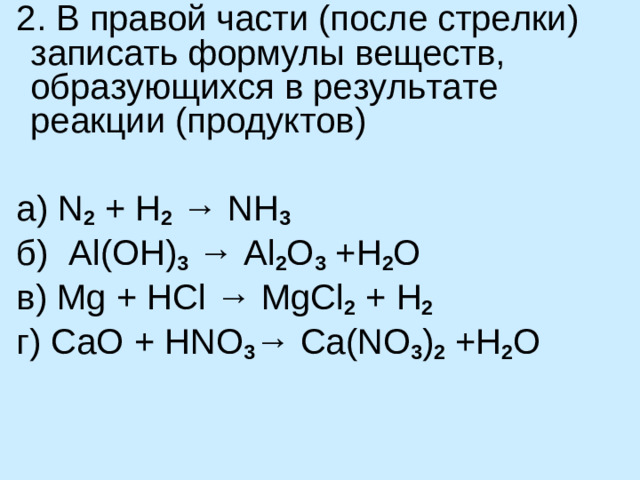
2. В правой части (после стрелки) записать формулы веществ, образующихся в результате реакции (продуктов)
а) N 2 + H 2 → NH 3
б) Al ( OH ) 3 → Al 2 O 3 + H 2 O
в) Mg + HCl → MgCl 2 + H 2
г ) С aO + HNO 3 → Ca(NO 3 ) 2 + H 2 O

3. Уравнение реакции составляется на основе закона сохранения массы веществ, т. е. слева и справа должно быть равное число атомов. Это достигается расстановкой коэффициентов перед формулами веществ.
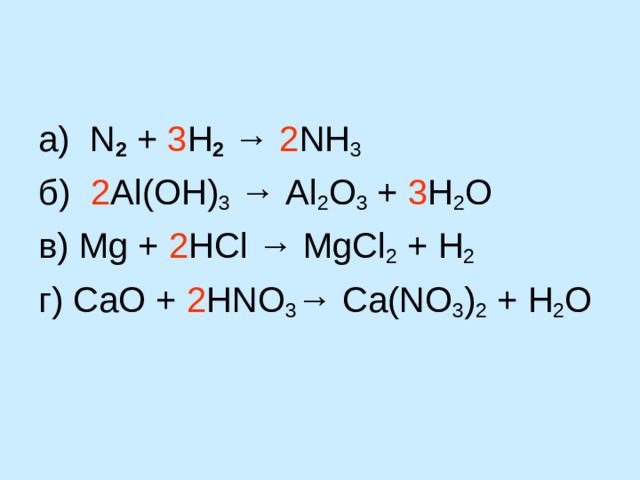
а) N 2 + 3 H 2 → 2 NH 3
б) 2 Al ( OH ) 3 → Al 2 O 3 + 3 H 2 O
в) Mg + 2 HCl → MgCl 2 + H 2
г) С aO + 2 HNO 3 → Ca ( NO 3 ) 2 + H 2 O
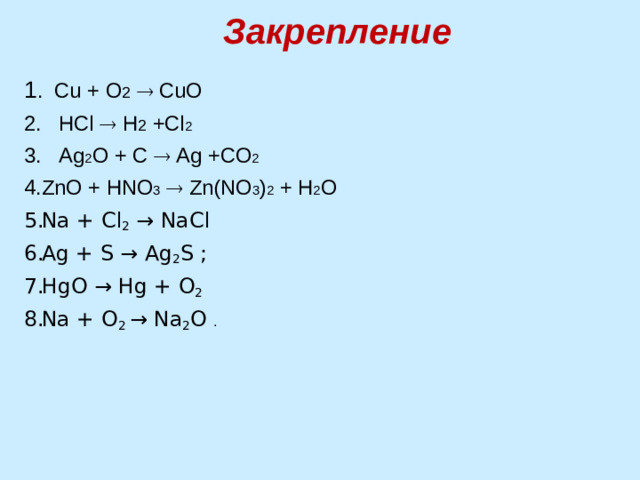
Закрепление
1 . Cu + O 2 CuO
2. HCl H 2 +Cl 2
3. Ag 2 O + C Ag +CO 2
- ZnO + HNO 3 Zn(NO 3 ) 2 + H 2 O
- Na + С l 2 → NaС l
- Аg + S → Аg 2 S ;
- НgО → Нg + О 2
- Na + О 2 → Nа 2 О .
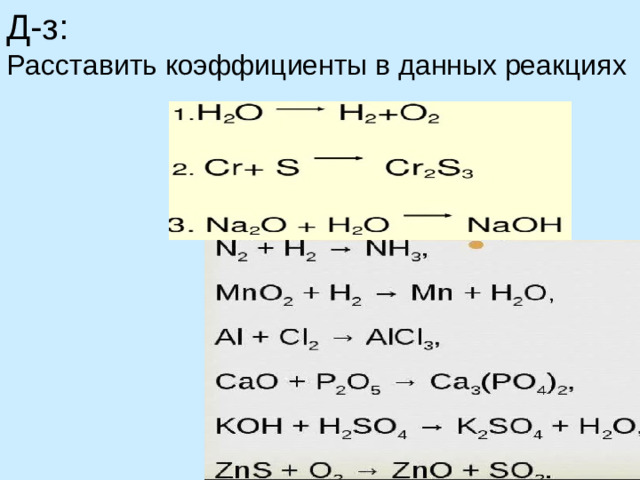
Д-з:
Расставить коэффициенты в данных реакциях







